
ГЛИЦИН CAS 56-40-6 изготовителя фабрики Китая самый большой для доставки запаса
-
Очищенность99,9%
-
ПользаЗдравоохранение
-
НачалоКитай
-
Пакет1KG/Tin 25KG/Drum*Carton
-
ИзготовительCO. РУКОВОДИТЕЛЯ СИАНЬ БИОХИМИЧЕСКОЕ ПРОЕКТИРУЯ, LTD
-
Место происхожденияКитай
-
Фирменное наименованиеLeader
-
СертификацияISO,GMP,SGS,HALA,KOSER,HACCP
-
Номер моделиLD
-
Количество мин заказа25KGS
-
ЦенаNegotiate Depend on order quantity
-
Упаковывая детали25KG/Drum
-
Время доставки2-3 рабочего дня
-
Условия оплатыЗападное соединение, MoneyGram, T/T, L/C
-
Поставка способности10MTS/Month
ГЛИЦИН CAS 56-40-6 изготовителя фабрики Китая самый большой для доставки запаса
| Элементарные сведения глицина |
| Название продукта: | Глицин |
| Синонимы: | ЗАКРЫВАТЬ БУФЕР; USP24 ГЛИЦИН USP24; ГЛИЦИН ТЕХНИЧЕСКИЙ; ГЛИЦИН USP; Глицин (ранг питания); Глицин (качество еды); Глицин (ранг Pharm); Глицин (ранг техника) |
| CAS: | 56-40-6 |
| MF: | C2H5NO2 |
| MW: | 75,07 |
| EINECS: | 200-272-2 |
| Категории продукта: | API; Аминокислота; Альф-амино кислоты; Реагенты для электрофореза; Аминокислоты; амино; Глицин [Gly, g]; Аминокислоты и производные; Аминокислоты; Биохимия; Омег-Aminocarboxylic кислоты; Омег-функциональные алканолы, карбоксильные кислоты, амины & галоиды; Глицин; Benzothiazoles, Thiazoles; Приемное устройство GABA/Glycine; Аминокислоты & производные |
| Mol файла: | 56-40-6.mol |
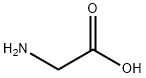 |
|
| Химические свойства глицина |
| Точка плавления | °C 240 (декабрь.) (LIT.) |
| Температура кипения | 233°C |
| плотность | 1,595 |
| давление пара | 0,0000171 PA (°C 25) |
| FEMA | 3287 | ГЛИЦИН |
| R.I. | 1,4264 (оценка) |
| Fp | 176.67°C |
| temp хранения. | 2-8°C |
| растворимость | H2O: 100mg/mL |
| форма | порошок |
| pka | 2,35 (на 25℃) |
| цвет | <5> |
| Запах | Непахучий |
| ПЭ-АШ | 4 (0,2 водного раствора моляра) |
| Ряд ПЭ-АШ | 4 |
| Растворимость воды | 25 g/100 mL (ºC 25) |
| λmax | λ: 260 nm Amax: 0,05 λ: 280 nm Amax: 0,05 |
| Номер JECFA | 1421 |
| Merck | 14,4491 |
| BRN | 635782 |
| Стабильность: | Конюшня. Горючий. Несовместимый с сильными окисляя агентами. |
| InChIKey | DHMQDGOQFOQNFH-UHFFFAOYSA-N |
| Ссылка базы данных CAS | 56-40-6 (ссылка базы данных CAS) |
| Ссылка химии NIST | Глицин (56-40-6) |
| Система канцелярии вещества EPA | Глицин (56-40-6) |
| Информация о безопасности |
| Заявления риска | 33 |
| Заявления безопасности | 22-24/25 |
| WGK Германия | 2 |
| RTECS | MB7600000 |
| TSCA | Да |
| Код HS | 29224910 |
| Опасные данные по веществ | 56-40-6 (опасные данные по веществ) |
| Токсичность | LD50 устно в кролике: 7930 mg/kg |
| Данные по MSDS |
| Поставщик | Язык |
|---|---|
| Monazol | Английский |
| Использование и синтез глицина |
| Аминокислоты с самой простой структурой | Глицин самой простой структуры в 20 членах серий аминокислоты, также известных как амино ацетат. Это не-необходимая аминокислота для человеческого тела и содержит и кислотную и основную функциональную группу внутри своей молекулы. Оно показывает как сильный электролит водный раствор, и имеет большую растворимость в сильных приполюсных растворителях но почти неразрешимый в неполярных растворителях. Кроме того, оно также имеет относительные высокие точку плавления и температуру кипения. Регулировка пэ-аш водного раствора может сделать экспонатом глицина различные молекулярные формы. Бортовая цепь глицина содержит только атом водорода. Вследствие другого атома водорода соединяясь с атомом α-углерода, глицин нет оптически изомера. В виду того что бортовое скрепление глицина очень небольшое, оно может занять космос который не может быть занят другими аминокислотами, как те аминокислоты расположенные внутри винтовая линия коллагена. На комнатной температуре, оно показывает как белые кристаллическое или светлый - желтый кристаллический порошок и имеет уникальный сладкий вкус который может облегчить вкус кислоты и алкалический вкус, маскируя горький вкус сахарина в еде и увеличить сладость. Однако, если чрезмерное количество глицина поглощено телом, то они не только не могут полностью быть поглощены телом, а также сломают баланс абсорбции тела аминокислот так же, как повлияют на абсорбцию других видов аминокислот, водящ к разницам питательного вещества и отрицательно затронутому здоровью. Напиток молока с глицином быть главной консервной банкой сырья легко вредит к нормальным росту и развитию молодых людей и детей. Он имеет плотность 1,1607, точку плавления °C 232~236 (декомпозиция). Он soluble в воде но неразрешим в алкоголе и эфире. Он способен на действовать вместе с хлористо-водородной кислотой для того чтобы сформировать соль хлоргидрата. Он в мышцах животных. ИТ можно произвести от реакции между ацетатом monochloro и нашатырным спиртом так же, как от гидролиза студневания с более дальнеишим рафинировкой. |
| История открытия | Аминокислоты органические кислоты содержа аминовую группу и основные блоки протеина. Они вообще бесцветные кристаллы с относительной высокой точкой плавления (°C сверх 200). Оно soluble в воде с amphiprotic характеристиками ионизацией и может иметь чувствительную колориметрическую реакцию с реагентом нингидрина. В 1820, глицин с самой простой структурой сперва был открыт в продукте гидролиза протеина. До 1940, не будет найдено что были около 20 видов аминокислот в природе. Они необходимы для синтеза протеина как человеческого, так и животного. Они главным образом типа α L аминокислоты. Согласно различному числу аминовых групп и карбоксильных групп, который содержат в аминокислотах, мы классифицируем аминокислоты в нейтральные аминокислоты (глицин, аланин, лейцин, изолейцин, валин, цистин, цистеин, метионин, треонин, серин, фенилаланин, тирозин, триптофан, пролин и оксипролин, etc.) с молекулами аминокислоты содержа только одну аминовую группу и карбоксильную группу; кислотная аминокислота (глутамат, аспартат) которая содержит 2 карбоксильного и одной аминовой группы; алкалические аминокислоты (лизин, аргинин) которая молекулярно содержит одну карбоксильную группу и 2 аминовой группы; Гистидин содержит кольцо азота которое показывает слабо алкалическое и таким образом также принадлежать к алкалическим аминокислотам. Аминокислоты можно получить и от гидролиза протеина и от химического синтеза. С 1960s, промышленное производство главным образом приложило микробное заквашивание, как фабрика мононатриевого глутамата получало широкое применение метод заквашивания для продукции глутамата. В последние годы, люди также приложили углероды нефти и другие химические продукты как сырье заквашивания для продукции аминокислот. Вышеуказанная информация отредактирована Chemicalbook Dai Xiongfeng. |
| Анализ содержимого | Точно весьте 175 mg образца который прошел засыхание для 2 h на °C 105 и устанавливает его в склянке 250m1, добавляет 50 mL ледяной уксусной кислоты для растворять; добавьте 2 падения решения теста кристаллического фиолетового (TS-74); титруйте с надхлорной кислотой 0.1ml/L к зеленоголубой критической точке. В то же время унести слепой опыт, и сделать необходимые коррекции. Каждый mL надхлорной кислоты 0.1mol/L соответствующий к глицину (C2H5NO2) 7.507mg. |
| Биосинтез продукции глицина | В конце 1980-х годов, Мицубиси Корпорация Японии добавил экранированный аэробный род Agrobacterium, Brevibacterium, коринебактерии к средству содержа углерод, азот и неорганический питательный раствор для культивирования, и после этого приложил этот класс бактерий для преобразовывать этаноламин к глицину в значении °C 25~45 и пэ-аш от 4 до 9 и более дополнительной прикладной концентрации, обработке ионной реакции обезвреживания для того чтобы получить продукт глицина. После входа 1990s, был новый прогресс на технологии производства глицина в зарубежных странах. Химическая промышленность Co Nitto (Япония) добавляет выращиванный в питательной среде: род псевдомонасов, род бактерий казеина, и род alcaligenes и другой вид в 0,5% (массовые часть, вес в сухом состоянии) к матрице глицина амин-содержа для реакции 45 h под значением °C 30 и пэ-аш 7,9 к 8,1 с почти всем амином глицина будучи hydrolyzed в глицин с конверсионным курсом 99%. Хотя биологические методы все еще в этапе исследования, однако, вследствие своей высокой селективности, свойство не-загрязнения, будет синтетическим маршрутом с сильно потенциалом развития. |
| Пользы |
|
| Описание | Глицин (сокращенный как Gly или g) органическое соединение с формулой NH2CH2COOH. Иметьзаместительводоподакаксвоясторон-цепь, глицинсамые небольшие20аминокислотобыкновеннонаходивпротеинах. СвоикодоныGGU, GGC, GGA, GGGгенетическогокода. Глицин бесцветное, твердое тело сладк-дегустации кристаллическое. Он уникален среди proteinogenic аминокислот в этом он не хирален. Он может поместить в гидрофильные или гидродобные окружающие среды, должные к своей минимальной бортовой цепи только одного атома водорода. Глицин также род имя завода сои (имени = глицина вида максимального). |
| Химические свойства | Белый, непахучий, кристаллический порошок имея sweetish вкус. Свое решение кислая реакция на лакмус. Один g растворяет в около 4 mL воды. Он очень немножко soluble в алкоголе и в эфире. Глицин может быть подготовлен от хлоруксусной кислоты и амиака; от источников протеина, как фиброин желатина и шелка; от гидрокарбоната аммония и цианида натрия; каталитическим расщеплением серина; от бромоводородные кисловочного и methyleneaminoacetonitrile. |
| Химические свойства | Глицин непахуч и имеет немножко сладкий вкус. |
| Химические свойства | Белый или почти белый, кристаллический порошок |
| Химические свойства | Глицин происходит как белый, непахучий, кристаллический порошок, и имеет сладкий вкус. |
| Возникновение | Fbroin желатина и шелка по сообщениям самые лучшие естественные источники этой аминокислоты |
| Пользы | глицин аминокислота используемая как texturizer в косметических образованиях. Он составляет приблизительно 30 процентов молекулы коллагена. |
| Пользы | Глицин несущественная аминокислота которая действует как питательное вещество и пищевая добавка. он имеет растворимость 1 g в 4 ml воды и обилен в коллагене. он использован для того чтобы замаскировать горький привкус charin sac, например, в искусственно услащенных лимонадах. он задерживает прогорклость в развитии в сале. |
| Пользы | Не-необходимая аминокислота для человеческого развития. Inhibitory нейротрансмиттер в спинном мозге, allosteric регуляторе приемных устройств NMDA. |
| Пользы | Глицин не-необходимая аминокислота для человеческого развития. Глицин inhibitory нейротрансмиттер в спинном мозге, allosteric регуляторе приемных устройств NMDA. |
| Пользы | В США, глицин типично продан в 2 рангах: Фармакопея Соединенных Штатов («USP "), и техническая ранг. Большинств глицин изготовлен как материал ранга USP для разнообразных польз. Продажи ранга USP определяют приблизительно 80 до 85 процентов рынка США для глицина. Фармацевтический глицин ранга произведен для некоторых фармацевтических применений, как внутривенные впрыски, где требования к очищенности клиента часто превышают минимум необходимы под обозначением ранга USP. Фармацевтический глицин ранга часто произведен к собственническим спецификациям и типично продан на награде над глицином ранга USP. Технический глицин ранга, который может или не может соотвествовать ранга USP, продан для пользы в промышленных применениях; например, как агент в металле complexing и заканчивать. Технический глицин ранга типично продан на скидке к глицину ранга USP. Животная и человеческая еда Другие рынки для глицина ранга USP включают свою пользу добавка в корме для домашних животных и корме для животных. Для людей, глицин продан как подсластитель/усиливающий агент вкуса. Некоторые дополнения еды и напитки протеина содержат глицин. Некоторые образования лекарства включают глицин для того чтобы улучшить гастрическую абсорбцию лекарства. Косметики и разносторонние применения Глицин служит как амортизируя агент в antacids, аналгетиках, antiperspirants, косметиках, и гигиенических косметикаах. Много разносторонних продуктов используют глицин или свои производные, как продукция резиновых продуктов губки, удобрения, complexants металла. Запас подачи реагентов Глицин промежуточное звено в синтезе разнообразие химических продуктов. Он использован в изготовлении глифосата гербицида. Глифосат неселективный внутрирастительный гербицид используемый для того чтобы убить засорители, особенно perennials и передачу или используемый в обработке cutstump как гербицид лесохозяйства. |
| Способы производства | Глицин был открыт в 1820, Henri Braconnot который закипел желатин с масляной серной кислотой. Глицин изготовлен промышленно путем обрабатывать хлоруксусную кислоту с амиаком: ClCH2COOH+2NH3Cl→H2NCH2COOH + NH4 Около 15 миллионов kg произведены ежегодно таким образом. В США (GEO Специальностью Химикатами, Inc.) и в Японии (Shoadenko), глицин произведен через синтез аминокислоты Strecker. |
| Способы производства | Химический синтез самый соответствующий метод подготовки глицина. Аминирование хлоруксусной кислоты и гидролиз aminoacetonitrile благоволить к методы продукции. |
| Подготовка | От хлоруксусной кислоты и амиака; от источников протеина, как fbroin желатина и шелка; от гидрокарбоната аммония и цианида натрия; каталитическим расщеплением серина; от бромоводородные кисловочного и methyleneaminoacetonitrile. |
| Определение | ChEBI: Самая простая (и единственная achiral) proteinogenic аминокислота, с атомом водорода как своя бортовая цепь. |
| Биосинтез | Глицин не необходим к человеческой диете, по мере того как он biosynthesized в теле от серина аминокислоты, который в свою очередь выведен от глицерата phospho 3. В большинств организмах, трансфераза серина энзима окси метиловая катализирует это преобразование через фосфат пиридоксаля сомножителя: серин + tetra гидро folate глицин +N5 →, n10-tetrahydrofolateметилена+H2O В печени позвоночных животных, синтез глицина катализирован synthase глицина (также вызвал энзим расщепления глицина). Это преобразование охотно реверзибельно: СО2 + NH4 + + n5, n10-folateметиленаtetraгидро+NADH+ глицинh +→ + tetrahydrofolate +NAD+ Глицин закодирован кодонами GGU, GGC, GGA и GGG. Большинств протеины включают только небольшие количества глицина. Примечательное исключение коллаген, который содержит глицин около 35%. |
| Biotechnological продукция | Глицин изготовлен исключительно химическим синтезом, и 2 основных процесса напрактикованы сегодня. Сразу аминирование хлоруксусной кислоты с большим избытком амиака дает хорошие выходы глицина без произведения большое количество di и trialkylated продуктов. Этот процесс широко использован в Китае, где главная программа глицина как сырье для глифосата гербицида. Другой основной процесс синтез Strecker. Сразу реакция Strecker цианида формальдегида и аммония производит ацетонитрил метилена амино, который необходимо hydrolyzed в 2 этапах для произведения глицина. Более эффективный подход к aminate промежуточные glycolonitrile, следовать гидролизом]. Альтернативный метод, который более часто приложен для гомологичных аминокислот, реакция Bucherer-айсбергов. Реакция формальдегида и углеаммонийной соли или гидрокарбоната дает промежуточный гидантоин, который можно hydrolyzed к глицину в отдельном шаге. |
| Биологические функции | Основная функция глицина как прекурсор к протеинам. Также строительный блок к многочисленным натуральным продучтам. Как биосинтетическое промежуточное звено В более высоких эукариотах, D-Aminolevulinic кислота, ключевой прекурсор к порфиринам, biosynthesized от глицина и succinyl-CoA. Глицин обеспечивает центральныйсубблок c2nвсехпуринов. Как нейротрансмиттер Глицин inhibitory нейротрансмиттер в центральной нервной системе, особенно в спинном мозге, стволе мозга, и сетчатке. Когда приемные устройства глицина активированы, хлорид входит в нейрон через ionotropic приемные устройства, причиняя Inhibitory postsynaptic potentia (IPSP). Стрихнин сильный антагонист на ionotropic приемных устройствах глицина, тогда как bicuculline слабое одно. Глицин необходимое coagonist вместе с глутаматом для приемных устройств NMDA. В отличие от inhibitory роли глицина в спинном мозге, это поведение облегчено на (NMDA) glutaminergic приемных устройствах которые excitatory. LD50 глицина 7930 mg/kg в крысах (устных), и оно обычно причиняет смерть hyperexcitability. |
| Биологические функции | Глицин другой inhibitory нейротрансмиттер CNS. Тогда как GABA расположено главным образом в мозге, глицин найден большей частью в вентральном рожке спинного мозга. Относительно знаны, что взаимодействуют немногие лекарства с глицином; самый знаменитый пример convulsant стрихнин агента, который кажется, что будет относительно специфическим антагонистом глицина. |
| Общее описание | Белые кристаллы. |
| Реакции воздуха & воды | Расстворимый в воде. |
| Профиль реактивности | Аминокислота. Водный раствор 0.2M имеет пэ-аш 4,0. , так действует как слабая кислота. Имеет характеристики как кисловочного, так и низкопробного. |
| Опасность | Польза в салах ограниченных до 0,01%. |
| Опасность пожара | НИЗКИЙ УРОВЕНЬ. Воспламеняет на очень высоких температурах. |
| Фармацевтические применения | Глицин по заведенному порядку использован как cofreeze-высушенный excipient в образованиях протеина вследствие своей способности сформировать сильную, пористую, и элегантную структуру торта в окончательном лиофилизованном продукте. Он один из наиболее часто используемых excipients в замораживани-высушенных вводимых образованиях вследствие своих выгодных freeze-drying свойств. Глицин был расследован как accelerant развала в быстро-дезинтегрируя образованиях вследствие своей превосходной моча природы. Он также использован как амортизируя агент и проводник в косметиках. Глицин может быть использован вместе с antacids в обработке гастрического hyperacidity, и он может также быть включен в подготовках аспирина для помощи уменьшения гастрического раздражения. |
| Аграрные пользы | Глицин самые простые естественно - происходя аминокислота и состав большинств протеинов. Своя формула h2n·CH2·COOH. |
| Биологическая деятельность | Один из главных inhibitory нейротрансмиттеров в относящийся к млекопитающим CNS, большей частью активное в спинном мозге и мозговом стволе. Также действует как модулятор/демодулятор excitatory передачи аминокислоты посредничанной приемными устройствами NMDA. Также доступный как часть приемного устройства NMDA - места Tocriset™ глицина. |
| Профиль безопасности | В меру токсический внутривенным маршрутом. Слабо токсический заглатыванием. Данные по перегласовки сообщили. Нагреванный к декомпозиции она испускает токсические перегары NOx. |
| Безопасность | Глицин использован как подсластитель, агент буферизации, и пищевая добавка. Чистая форма глицина в меру токсическая маршрутом IV и слабо токсическая заглатыванием. Внутрирастительная абсорбция решений полива глицина может привести к помехам жидкости и электролитного баланса и сердечнососудистых и легочных разладов. LD50 (мышь, IP): 4,45 g/kg LD50 (мышь, IV): 2,37 g/kg LD50 (мышь, устные): 4,92 g/kg LD50 (мышь, SC): 5,06 g/kg LD50 (крыса, IV): 2,6 g/kg LD50 (крыса, устные): 7,93 g/kg LD50 (крыса, SC): 5,2 g/kg |
| хранение | Глицин начинает разложить в магазине 233°C. в хорошо закрытых контейнерах. Решения полива глицина (глицин 95-105%) следует сохранить в одиночных контейнерах дозы, предпочтительно типе я или типе стекле II. |
| Методы очищения | Выкристаллизовывайте глицин от дистиллированной воды путем растворять на 90-95o, фильтровать, охлаждать к около -5o, и стекать кристаллы центробежно. Альтернативно, выкристаллизовывайте его от дистиллированной воды добавлением MeOH или EtOH (например 50g растворило в 100mL теплой воды, и добавлено 400mL MeOH). Кристаллы помыты с MeOH или EtOH, после этого с диэтиловым эфиром. Правоподобные примеси glycinate аммония, iminodiacetic кислота, нитрилотриуксусная кислота или/и хлористый аммоний. [Greenstein & Winitz химия аминокислот J. Wiley, VOL. 3 p 1955 1961, Beilstein 4 IV 2349.] |
| Ухудшение | Глицин ухудшен через 3 тропы. Преобладающая тропа в животных и растениях включает глицин энзима расщепления глицина + tetra гидро folate + СО2 NAD + → + NH4+ + n5, n10-hydrofolateметиленаtetra+NADH+H+во второйтропе, глицинухудшеныв2шагах. Первый шагобратныйбиосинтезаглицинаотсеринастрансферазойсеринаоксиметильной. Серинпосле этогопреобразованкпируватудегидратазойсерина. Втретейтропеухудшенияглицина, глицинпреобразованкглиоксилатуD-аминокисловочнойоксидазой. Глиоксилатпосле этогоокисленпеченочнойдегидрогеназойлактатакоксалатув реакцииNAD +-dependent. Полувыведение глицина и своего исключения от тела меняет значительно основанный на дозе. В одном исследовании, полувыведение находилось между 0,5 и 4,0 часами. |
| Присутсвие в космосе | Было дебатировать обнаружение глицина в межзвездной среде. В 2008, глицин - как нитрил aceto молекулы амино открыл в большой молекуле Heimat, гигантском облаке газа около галактического центра в Стрелце созвездия максимальным институтом Planck для радио-астрономии. В 2009, был подтвержен глицин попробованный в 2004 от кометы дикие 2 кораблем Stardust NASA, первое открытие внеземного глицина. Результаты этой миссии поддержали теорию panspermia, которое требует что «семена» жизни широко распространенный повсеместно во вселенная. |
| Несовместимости | Глицин может пройти реакции Maillard с аминокислотами для произведения желтеть или коричневеть. Сахара уменьшения также будут взаимодействовать с вторичными аминами для того чтобы сформировать имин, но без любого сопровождая желт-коричневого обесцвечивания. |
| Регулирующее состояние | GRAS перечислило. Принятый для пользы как пищевая добавка в Европе. Включенный в базе данных ингредиентов УПРАВЛЕНИЯ ПО САНИТАРНОМУ НАДЗОРУ ЗА КАЧЕСТВОМ ПИЩЕВЫХ ПРОДУКТОВ И МЕДИКАМЕНТОВ неактивной (IM, IV, впрыски SC; устный; ректальный) и одобренный для irrigant решений. Включенный в парентральном (порошки для впрыски; решения для впрыски; вакцины; наборы для имплантируют) и nonparenteral (orodispersible планшеты/устное lyophilizate; порошки для вдыхания; порошки для устного решения; образования планшетов) лицензированные в Великобритании. |
| Продукты и сырье подготовки глицина |
