| Описание |
См. MONOCHLORIDE ι-ЛИЗИНА. |
| Химические свойства |
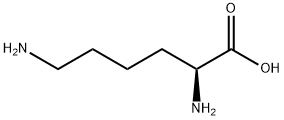
L-лизин необходимая аминокислота (строительный блок протеина) которая не может быть произведена телом от других ents nutri. Он помогает обеспечить адекватную абсорбцию кальция и образование коллагена для косточки, хрящевины и соединительной ткани. Эта смесь непахуча. |
| Химические свойства |
Белый к светлоому-желт кристаллическому порошку |
| Возникновение |
Некоторые естественные источники еды для l-лизина включают фасоли Лимы, фасоли почки, картошки, мозоль, красное мясо, рыб и молоко. |
| Пользы |
Необходимая аминокислота для человеческого развития. Выпарки лизина полезны в много клетчатых процессов, должных к их способности признавать большое разнообразие пост-поступательных изменений. |
| Пользы |
Умеренный антагонист серотонина и необходимая аминокислота. |
| Пользы |
лизин кож-подготовляя аминокислота. |
| Определение |
ChEBI: L-альф-амино кислота; L-изомер лизина. |
| Подготовка |
Произведенный заквашиванием. Также произведенный при помощи непрерывной технологии ионной реакции. |
| Biotechnological продукция |
Glutamicum и, в меньшей степени, Escherichia Coli C. основные организмы используемые сегодня для промышленной продукции L-лизина. Первые L производящие напряжения основанные на glutamicum C. были сообщены в 1961, и тех основанных на Escherichia Coli в 1995. Преимущества использования Escherichia Coli против glutamicum C. включают достижение более высоких темпов роста на более высоких температурах заквашивания. Образование лизина сильно повлияно на 2 энзимами, киназой аспартата (AK) и дегидрогеназами homoserine (HDH). AK преобразовывает аспартат в semialdehyde аспартата, и сильно обратн-заблокировано лизином и треонином. HDH преобразовывает semialdehyde аспартата в homoserine, который промежуточное звено для биосинтеза треонина, метионина, и изолейцина. L Лизин производящие напряжения поэтому часто содержат прекращанное регулирование AK и/или уменьшенную деятельность HDH. Несмотря на улучшение потока от аспартата к лизину, наличие ключевых метаболитов от центральных метаболически троп также необходимо. Здесь образование oxaloacetate сразу от пирувата phosphoenol или через пируват необходимо для выхода углерода по мере того как некоторые ненужные циклы включены. Например, инактивирование carboxykinase пирувата phosphoenol энзима, который катализирует обратную реакцию от oxaloacetate к пирувату phosphoenol дало улучшение в образовании лизина. overexpression карбоксилазы пирувата, выход преобразования глюкозы к лизину смог быть увеличен 50%. С напряжением синтетического лизина hyperproducing, содержа 12 определенных изменения от дикого типа, выход углерода 0,55 g/g и титр продукта 120 G/L над заквашиванием 30 h смогли быть получены.
Сегодня, однако, основной коммерчески процесс для L-лизина остается заквашиванием glutamicum C. Это выполнено в режиме питать-серии в широкомасштабных ферментерах до 500 томов m3, с производственными мощностями свыше 100 000 тонн. Коммерчески процесс производства всесторонне был описан Pfefferle. |
| Пороговые значения ароматности |
Обнаружение: 500 ppm |
| Ссылки синтеза |
Журнал американского химического общества, 71, P. 3161, 1949 DOI: 10.1021/ja01177a063 |
| Профиль безопасности |
Экспириментально teratogen. Экспириментально воспроизводственные влияния. Нагреванный к декомпозиции он испускает токсические перегары NOx. |
| Ветеринарные лекарства и обработки |
Лизин может быть эффективен в подавлять инфекции FHV-1 в котах. |
| Методы очищения |
Выкристаллизовывайте L-лизин от водного EtOH. [Greenstein & Winitz химия аминокислот J. Wiley, VOL. 3 pp 2097-2122 1961, Kearley & Ingersoll j до полудня Chem Soc 73 5783 1951, Beilstein 4 IV 2717.] |