| Элементарные сведения имидазола |
| метод подготовки главной программы физических характеристик химических свойств использует способ производства |
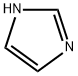
| Название продукта: | Имидазол |
| Синонимы: | 1H-IMIDAZOLE; 1,3-DIAZA-2,4-CYCLOPENTADIENE; 1,3-DIAZOLE; LABOTEST-BB LTBB001344; БУФЕР ИМИДАЗОЛА; IMINAZOLE; ИМИДАЗОЛ; GLYOXALIN |
| CAS: | 288-32-4 |
| MF: | C3H4N2 |
| MW: | 68,08 |
| EINECS: | 206-019-2 |
| Категории продукта: | API; Фармацевтические промежуточные звена; Сильно очищенные реагенты; Другие категории; Зона уточнила продукты; Буфер; Имидазолы, пирролы, пиразолы, пирролидоны; Биохимия; Реагенты для синтеза олигосахарида; Буфера ранга ACS; Ранг ACS; Биологические буфера; Буфера a к z; Промежуточное звено для хлоргидрата Propafenone.; Строительные блоки; C3 к C8; Химический синтез; Необходимые химикаты; Гетероциклические строительные блоки; Имидазолы; Неорганические соли; Предметы первой необходимости исследования; Решения и реагенты; 2-8°C |
| Mol файла: | 288-32-4.mol |
 |
|
| Химические свойства имидазола |
| Точка плавления | 88-91 °C (LIT.) |
| Температура кипения | °C 256 (LIT.) |
| плотность | 1,01 g/mL на °C 20 |
| давление пара | <1 mm="" Hg=""> |
| R.I. | 1,4801 |
| Fp | °F 293 |
| temp хранения. | 2-8°C |
| растворимость | H2O: 0,1mна°C20, ясный, бесцветном |
| форма | кристаллический |
| pka | 6,953 (на 25℃) |
| цвет | белый |
| Удельный вес | 1,03 |
| Запах | Подобие амина |
| ПЭ-АШ | 9.5-11.0 (25℃, 50mg/mL в H2O) |
| Ряд ПЭ-АШ | 9.5 - 11 |
| Растворимость воды | 633 G/L (ºC 20) |
| λmax | λ: 260 nm Amax: 0,10 λ: 280 nm Amax: 0,10 |
| Чувствительный | Водоемкий |
| Merck | 14,4912 |
| BRN | 103853 |
| Стабильность: | Конюшня. Несовместимый с кислотами, сильными окисляя агентами. Защитите от влаги. |
| InChIKey | RAXXELZNTBOGNW-UHFFFAOYSA-N |
| Ссылка базы данных CAS | 288-32-4 (ссылка базы данных CAS) |
| Ссылка химии NIST | 1H-Imidazole (288-32-4) |
| Система канцелярии вещества EPA | Имидазол (288-32-4) |
| Информация о безопасности |
| Коды опасности | C, XI, t |
| Заявления риска | 36/38-63-34-22-20/21/22-61 |
| Заявления безопасности | 26-36/37/39-45-22-36-27-53 |
| RIDADR | ООН 2923 8/PG 3 |
| WGK Германия | 1 |
| RTECS | NI3325000 |
| Температура самогорения | °C 480 |
| TSCA | Да |
| HazardClass | 8 |
| PackingGroup | III |
| Код HS | 29332990 |
| Токсичность | LD50 в мышах (mg/kg): 610 i.p.; 1880 устно (Nishie) |
| Данные по MSDS |
| Поставщик | Язык |
|---|---|
| SigmaAldrich | Английский |
| ACROS | Английский |
| АЛЬФА | Английский |
| Использование и синтез имидазола |
| химические свойства | Имидазол между 2 атомами азота содержания 5 membered гетероциклического смесей. Unshared пара электрона 1 сдержанного атома азота в кольце имидазола участвует в циклическом спряжении, уменьшает плотность электронов атома азота, и делает водопод атома азота легко выходит в форме водопода. Поэтому имидазол имеет слабую кислотность, и может сформировать соль с сильным основанием. Unshared пара электрона 3 сдержанного атома азота в кольце имидазола не делает участвует в циклическом спряжении, пока она занимает орбиталь гибридизированную sp2, может принять протоны, и соль формы с сильной кислотой. Алкалический имидазола немножко более сильна чем пиразол и пиридин. Tautomerism в кольце имидазола. Водопод на 1 сдержанном атоме азота можно перенести к атому 3, поэтому, производные имидазола с таким же заместителем соответственно на бит 4 бите и 5 tautomers. Имидазол стабилизирован к кислоте, и имеет деятельность при противоокислительного. Производные имидазола широко найдены в природе, как гистамин, гистидин и бензимидазол, etc. Некоторые интересные реагенты в смесях имидазола ацила. Например, 1 имидазол ацетила стабилизированный acylating агент, после того как реакция с пирролом, им будет 1 пиррол ацетила. Furthermore, вообще, 1 имидазол ацетила может получить кетоны и альдегиды используя реагент и разбавитель Grignard. Реакция n, N-carbonyldimidazole и карбоксильного получит полезный имидазол ацила реагента. Отношение между имидазолом и естественными смесями очень близко. Например, кольцо пиримидина поворачивает в производные пурина после конденсации. В дополнение к быть как 6 амино пурин и гуанин нуклеиновые кисловочные основания, оно также существует в организмах мочевой кислоты, кофеина и теофиллина. Каталитическое действие имидазола, как ускоренный ход гидролиз энзима, все еще под исследованием. По мере того как причина аллергической кожи, своя токсичность подобное todiamine. Крыса устное LD501880mg/kg. 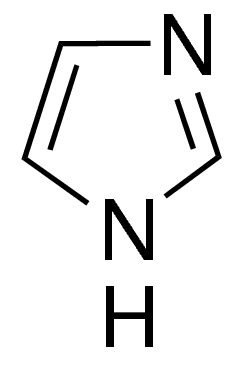 структура имидазола |
| Физические характеристики | В природе, только производные имидазола и никакой свободный имидазол. Высыпание от коксобензола бесцветная кристаллическая призма, с нюхами амиака. Относительные молекулярные массовые 68,08. Относительная плотность 1,0303 (101/4℃). Точка плавления 89~91℃, температура кипения 257℃, 165℃~168℃ (2.67×103Pa) и 138.2℃ (1.60×103Pa). Горячая точка 145℃. R.I. 1,4801 (101℃). Выкостность 2.696mPa·s (100℃). Немножко soluble в коксобензоле, эфире нефти, soluble в эфире, ацетоне, хлороформе и пиридине, легко soluble в воде (на нормальной температуре 70) и этаноле. Она появляется слабое алкалическое. Как -NH-скрепление на 1 скреплении and-N= укуса на скреплении водопода 3 сдержанном форм, температура кипения довольно высока; когда 1 сдержанный водопод заменен, скрепление водопода нельзя сформировать, следовательно температура кипения уменьшает. О термической стабильности, она редко растворяет под 250℃ (температура декомпозиции 590℃). Она также очень стабилизирована к разбавителю и оксиданту, но может сформировать стабилизированное соль с неорганической кислотой. Имеющ некоторые некоторые ароматичные свойства, также смогл получить галоидирование, нитрование, сульфуризацию и hydroxymethylation в присутствии к катализатору. Смогите быть соединено с тяжелым сдержанным солью азота в 2. К тому же, должный к =NH (1 биту) соединенному с 2 двойными связями, с некоторым из «кисловочного», оно может быть заменен металлом для того чтобы получить соль. К тому же, 3 сдержанных иона азота имеют влияние координации на ионах металла, которые могут сформировать смеси хелата. Хотя трудно восстановить, но может быть совмещено с протоном для генерации типа катиона со структурой резонанса, и получает стабилизированной формы. Tautomers кольца имидазола очень легко для изменения, поэтому это трудно сказать сдержанные сдержанные изомеры на 4 или 5. Вышеуказанная информация отредактирована Chemicalbook он Pu Liao. |
| Главная программа | Имидазол можно использовать как агент эпоксидной смолы леча, улучшить механические свойства как гнуть, протягивать и обжатие etc., улучшает электрические свойства изоляции, и улучшает представление свойств химической устойчивости, которое широко использовано в компьютерах и электроприборах; Использованный как антиржавейный агент для меди в платах с печатным монтажом и интегральных схемаах; Использованный как фармацевтическое сырье для изготовляя противогрибковых лекарств, противогрибковых агентов, лекарства для обработки hypoglycemia, искусственной плазмы, лекарства trichomonad, лекарства бронхиальной астмы, агента пятна, etc.; Использованный как сырье пестицида для синергетика, инсектицидов и фунгисидов борного кисловочного агента; К тому же, имидазол также использован как сырье агента смолы мочевин-формальдегида леча, фотографической медицины, прилипателя, покрытия, вулканизатора, противостатического агента, etc.; промежуточное звено для органического синтеза. |
| Метод подготовки | С глиоксалем как сырье, реактивное в сульфате формальдегида и аммония (или амиаке) в 85~90℃, и получите сульфат имидазола и после этого нейтрализованный с окисоводоподом кальция для того чтобы получить имидазолу незрелый продукт. Фильтровать, стирка воды, совмещающ фильтрат и стирки, концентрация и кристаллизация испарения понижения давления, тогда оно делали. Если использовать амиак сразу, тогда там должен быть никакими шагами обработки сульфата и его можно подготовить сразу. Или с сульфатом или амиаком аммония, выход относительно низок, приблизительно 45%. С o-фенилен-диамином и муравьиной кислотой как сырье, через циклизацию к бензимидазолу, и после этого через оксидацию в решении масляной серной кислоты для того чтобы произвести имидазол dicarbonyl; позже во влиянии медной оксидации, через декарбоксилирование от 100 к 150℃, который нужно получить незрелым; И после этого в рекристаллизации решения коксобензола для того чтобы получить имидазол законченный - продукты. С кислотой d-тартрата как сырье, в масляной серной кислоте, азотноводородная кислота была использована для того чтобы унести нитрификацию, и получает 2, кислота тартрата dinitro 3; и после этого в реакции формальдегида и амиака, получить двукарбоновый имидазол; в конце концов декарбоксилирование, который нужно получить его. |
| Пользы | 1.Used как промежуточное звено бактерицида для imazalil, prochloraz, etc., и что фармацевтических противогрибковых лекарства, econazole, ketoconazole, и clotrimazole также. 2.Used как органические синтетические материалы и промежуточные звена для подготовки лекарств и пестицидов. 3.Used как аналитический реагент, так же, как в органическом синтезе. 4.Imidazole главным образом использовано как леча агент для эпоксидной смолы. В Японии имидазол определяет половины потребления. Для смесей имидазола дозировка которых 0,5 до 10 процента эпоксидной смолы, ее можно использовать в противогрибковом лекарстве, агенте mildew муравья, hypoglycemic лекарстве, искусственной плазме, etc., также может быть использована в медицинах для того чтобы вылечить угорь trichomoniasis и индюка. Имидазол также одно из главного сырья во время продукции miconazole, econazole, clotrimazole и ketoconazole имидазола противогрибковых. имидазолом и 2, 4, ω-trichloroacetophenon как главное сырье, он может получить enilconazde фунгисида плода. Добавьте 2, 4, ω-trichloroacetophenon в абсолютный метанол, с рефлюксом топления, добавляя бром. Ожидание до тех пор пока цвет решения постепенно не исчезнет, охлаждая к 0℃, и после этого интенсивно смешивая его для 3h. И вакуумная перегонка метанола. Положите остальное жидкостное в воду, для того чтобы извлечь ее с dichloromethane. После выдержки взятой с dichloromethane, добавьте разбавьте азотноводородную кислоту для того чтобы получить соль; рекристаллизация с водой и после этого обработанная с амиаком для того чтобы получить 2', 4' - ацетофенон dichloro-2-imidazole. Furthermore уменьшение гидридобората натрия пользы в соответствуя алкоголи, и после этого в присутствии к окисоводоподу натрия и этанному формамиду, хлорид аллила пользы основанный для того чтобы получить enilconazde (также известное как enilconazole). после добавления для того чтобы разбавить соль и воду азотноводородной кислоты после рекристаллизации используя обработку аммиачной воды 2,2", 4" - кетон дихлорированного метилового имидазола 2 фениловый этиловый. Он имеет что-то в общем структуры и способов производства между enilconazde и miconazole. Miconazole агент широк-спектра противогрибковый, и enilconazde также противогрибковый агент, который широко использован в imazalil. 5.Agrochemical промежуточные звена, промежуточные звена бактерицида, фунгисид триазола. |
| Способ производства | 1.It можно сделать через циклизацию и обезвреживание глиоксалем. Положенный сульфат глиоксаля, формальдегида и аммония в бак реакции, шевелит и нагревает до 85-85℃ с консервацией 4h жары. Охладите его к 50-60℃, с обезвреживанием воды к пэ-аш для больше жара чем 10. до 85-90℃, экскреции амиака для больше чем 1h, охлаждает ее стирка немножко, фильтра и торта фильтра с горячей водой; Совмещенные мытье, фильтрат, и концентрация вакуума до безводного испаренного вне; не будет продолжать к вакуумной перегонке до низких кипя веществ совсем испарил вне, соберите (0.133-0.267kPa) части 105-160℃ и после этого имидазол сделан. Выход около 45%. Другой метод сделать циклизацию o-diaminobenzene и муравьиной кислоты для того чтобы получить бензимидазол, следовать 4, имидазол dyhydroxy 5 через реакцию и незамкнутая перекиси водорода, и в конце концов получить имидазол через декарбоксилирование. 4, имидазол dyhydroxy 5 также могут быть сделаны d-тартратом через нитрование и циклизацию. Процесс получать имидазол через декарбоксилирование 4, имидазол dyhydroxy 5 как ниже: смешивание 4, имидазол dyhydroxy 5 с медной окисью, жарой до 100-280℃, испускает серии газа углекислого газа, тогда собранный отгон незрелый продукт, и наконец рекристаллизует его с коксобензолом для того чтобы получить продукт, и выход 76%. способ производства 2.The положить сульфат глиоксаля, формальдегида и аммония в бак реакции, шевелит и нагревает до 85-85℃ с консервацией 4h жары. Охладите его к 50-60℃, с обезвреживанием воды к пэ-аш для больше жара чем 10. до 85-90℃, экскреции амиака для больше чем 1h, охлаждает ее стирка немножко, фильтра и торта фильтра с горячей водой; Совмещенные мытье, фильтрат, и концентрация вакуума до безводного испаренного вне; не будет продолжать к вакуумной перегонке до низких кипя веществ совсем испарил вне, соберите части 105~160℃/133~266Pa и после этого имидазол сделан. С o-фенилен-диамином как сырье, положите его в муравьиную кислоту, пошевелите и нагрейте вверх, консервация жары на 95~98℃ для 2h, охладите его к 50~60℃, отрегулируйте значение ПЭ-АШ до 10 с 10%NaOH; Когда оно достигает комнатную температуру, с фильтровать, мыть и сушить для того чтобы получить бензимидазол. Положенный бензимидазол в сконцентрированную масляную серную кислоту, жару до 100℃, и медленно падает в H2O2. Реакция пока шевелящ под 140~150℃ для 1h, охлаждая к 40℃, сделаны разбавление воды, высыпание, кристаллизация, фильтрация, мыть, сушить, и после этого 4, имидазол dyhydroxy 5. Смешивание 4, имидазол dyhydroxy 5 с медной окисью, жарой до 100-280℃, испускает серии газа углекислого газа, тогда собранный отгон продукт белого блока незрелый, и наконец рекристаллизует его с коксобензолом для того чтобы получить точный имидазол. |
| Химические свойства | Имидазол гетероциклическая смесь с 5-membered плоскостным кольцом. Он амфотерн и сильно приполюсн. Pharmacophore имидазола существует в bioactive смесях включая аминокислоты, регуляторы выращивания растения и терапевтические агенты. |
| Пользы | Превосходный для буферов в границах пэ-аш 6.2-7.8 Имидазол был использован
|
| Пользы | Имидазол разностороннее heterocycle используемое в подготовке различных биологически активных смесей как гистидин аминокислоты и присутствует в много противогрибковое лекарство. Также используемый ext ensively как антикоррозийное вещество на металлах переходной группы как медь. Оно использован в органическом синтезе и как antiirradiationagent. |
| Определение | ChEBI: Tautomer имидазола которое имеет водопод проникать на положении 1. |
| Опасность для здоровья | Оно более менее токсический по отношению к пирролу и otherfive-membered гетероциклическому ofnitrogen смесей. Внутрибрюшинное ofimidazole администрации причинило сомнолентность, сужения мышцы, и конвульсии в мышах. Значение Theoral LD50 в мышах в mg/kg range900. |
| Опасность пожара | Noncombustible твердое тело. |
| Методы очищения | Выкристаллизовывайте имидазол от *benzene, CCl4, CH2Cl2, EtOH, эфира любимца, эфира ацетона/любимца и дистиллированной деионизированной воды. Высушите его на 40o под вакуумом над P2O5. Дистиллируйте его на низком давлении. Оно также очищен сублимацией или плавить зоны. [VOL. III Snyder и др. Org Synth Coll 471 1955, Ber 97 Bredereck и др. Chem 827 1964, Caswell & Spiro j до полудня Chem Soc 108 6470 1986.] 15N-imidazole выкристаллизовывает от *benzene [Scholes и др. j до полудня Chem Soc 108 1660 1986]. [Beilstein 23 II 34, 23 III/IV 564, 23/4 v 191.] |
| Продукты и сырье подготовки имидазола |

