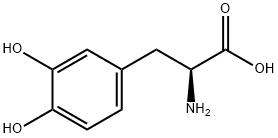
| Элементарные сведения Levodopa |
| |
| Химические свойства Levodopa |
| Точка плавления |
276-278 °C (LIT.) |
| альфа |
HCl (c=5.3, 1N) -11,7 º |
| Температура кипения |
334.28°C (примерный расчет) |
| плотность |
1,3075 (примерный расчет) |
| R.I. |
-12 HCl (C=5, 1mol/L) ° |
| temp хранения. |
2-8°C |
| растворимость |
Немножко soluble в воде, практически неразрешимой в этаноле (96 процентах). Он свободно soluble в хлористо-водородной кислоте 1 m и sparingly soluble в хлористо-водородной кислоте 0,1 m. |
| pka |
2,32 (на 25℃) |
| форма |
Кристаллический порошок |
| цвет |
Белый к сметанообразному |
| Растворимость воды |
Немножко soluble в воде, разбавляет хлористо-водородную кислоту и муравьиную кислоту. Неразрешимый в этаноле. |
| Merck |
14,5464 |
| BRN |
2215169 |
| Стабильность: |
Конюшня. Несовместимый с сильными окисляя агентами. Свет и воздух чувствительные. |
| InChIKey |
WTDRDQBEARUVNC-LURJTMIESA-N |
| Ссылка базы данных CAS |
59-92-7 (ссылка базы данных CAS) |
| Ссылка химии NIST |
Levodopa (59-92-7) |
| Система канцелярии вещества EPA |
Levodopa (59-92-7) |
| |
| Информация о безопасности |
| Коды опасности |
Xn |
| Заявления риска |
22-36/37/38-20/21/22 |
| Заявления безопасности |
26-36-24/25 |
| WGK Германия |
3 |
| RTECS |
AY5600000 |
| F |
10-23 |
| TSCA |
Да |
| Код HS |
29225090 |
| Опасные данные по веществ |
59-92-7 (опасные данные по веществ) |
| Токсичность |
LD50 в мышах (mg/kg): 3650 ±327 устно, 1140 ±66 i.p., 450 ±42 i.v., >400 s.c.; в мужских, женских крысах (mg/kg): >3000, >3000 устно; 624, 663 i.p.; >1500, >1500 s.c. (Clark) |
| |
| Использование и синтез Levodopa |
| Химические свойства |
Бесцветный кристаллический порошок |
| Инициатор |
Larodopa, Roche, США, 1970 |
| Пользы |
Естественный изомер немедленного прекурсора допамина; продукт гидроксилазы tyrsine |
| Пользы |
antiparkinsonian |
| Пользы |
Немедленный прекурсор допамина и продукт гидроксилазы тирозина. |
| Определение |
ChEBI: Оптически активная форма допы имея L-конфигурацию. Использованный для того чтобы обработать жесткость, треморы, спазмы, и плохое управление мышцы заболевания Parkinson |
| Процесс производства |
Обязанность 1 000 g из земных фасолей бархата была извлечена с 9 литрами кислоты 1% водной укусной на комнатной температуре над периодом 20 часов со случайной активностью во время первых 4 часов. Ликер был сцежен и thebean slurry пульпы был вакуумом фильтрованным через торт кислот-помытой диатомной земли в воронке Buechner. Сцеженный ликер был совмещен с фильтратом и был сконцентрирован под вакуумом и атмосферой азота к тому 900 ml. После обрабатывать с кислот-помытым активированным углем, концентрат после этого был фильтрован через кислот-помытую диатомную землю.
После концентрировать фильтрат до приблизительно 400 ml, твердые тела начали выкристаллизовывать вне в которое время фильтрат был охлажен путем refrigerating на 5°C на несколько часов. Фильтрация дала g 18,7 L-допы, MP 284° к 286°C (декабрю.); [α] d 8.81° (решение 1% в водном HCl 4%). Инфракрасный спектр и хромотография бумаги показали очень хорошую L-допу согласно патенту 3 253 023 США.
Различные синтетические маршруты также описаны Kleeman и Engel. |
| Фирменное наименование |
Bendopa (Valeant); Dopar (графство); Larodopa (Roche). |
| Терапевтическая функция |
Antiparkinsonian |
| Биологические функции |
Levodopa (L-DOPA), самое надежное и самое эффективное лекарство используемое в обработке паркинсонизма, можно рассматривать формой терапии замены. Levodopa биохимический прекурсор допамина. Оно использован для того чтобы повысить уровни допамина в neostriatum parkinsonian пациентов. Допамин сам не пересекает барьер кров-мозга и поэтому не имеет никакие влияния CNS. Однако, levodopa, как аминокислота, транспортировано в мозг транспортными системами аминокислоты, где оно преобразовано к допамину декарбоксилазой аминокислоты энзима L-ароматичной.
Если levodopa управлено самостоятельно, то оно обширно метаболизировано L-ароматичной декарбоксилазой аминокислоты в печени, почке, и желудочно-кишечном тракте. Для предотвращения этого периферийного метаболизма, levodopa coadministered с carbidopa (Sinemet), периферийным иом АБС битор декарбоксилазы. Levodopa сочетания из с carbidopa понижает необходимую дозу levodopa и уменьшает периферийные побочные эффекты связанные со своей администрацией.
Levodopa широко использовано для обработки всех типов паркинсонизма за исключением тех связанных с лекарственной терапией антипсихотика. Однако, по мере того как паркинсонизм развивает, продолжительность извлекает пользу из каждой дозы levodopa может сократить (нося- влияние). Пациенты могут также начать неожиданные, непрогнозируемые зыбкост между подвижностью и обездвиженность (включеный-выключеное влияние). В считанные минуты, наслаждаться пациента нормальная или почти нормальная подвижность может внезапно начать строгую степень паркинсонизма. Эти симптомы вероятно должны к прогрессированию заболевания и потери striatal терминалов нерва допамина. |
| Общее описание |
Первый значительный прорыв в обработке PDcame около с введением levodopa высоко-дозы. Fahn сослалось на это как революционное развитие intreating parkinsonian пациенты. Разумное объяснение для oflevodopa пользы для обработки PD было установлено в theearly 1960s. Показали, что имели Parkinsonian пациенты decreasedstriatal уровни DA и уменьшенного мочевыделительного excretionof DA. С тех пор, levodopa показало для того чтобы быть remarkablyeffective для обрабатывать симптомы действия PD.Because ofenzymatic MAO-A в желудочно-кишечном тракте (GI) и AADC в периферии, только небольшой процент (1%-2%) levodopa поставлен в CNS.Coadministration levodopa с иом АБС битор AADC, carbidopa, предотвращает декарбоксилирование levodopa вне CNS. Resultsin levodopa и carbidopa сочетания из значительное повышение в доставке DA к CNSwith уменшение в периферийных побочных эффектах. Долгосрочное levodopa therapywith водит к прогнозированным усложнениям мотора. Эти включают потерю эффективности перед следующей дозой («носящ "), зыбкост ответа мотора («включено-выключено "), andunwanted движения (дискинезии). Arethought этих влияний, который будет причинять невозможность therapyto levodopa восстановить нормальные уровни DA в CNS. в результате, theuse длинн-действуя агонистов DA может помочь parkinsonianpatients. |
| Биологическая деятельность |
Немедленный прекурсор допамина, произведенный гидроксилазой тирозина. Показывает antiParkinsonian деятельность. |
| Лекарствоведение |
В нескольких попыток зафиксировать дефицит допамина в паркинсонизме, введение сразу прекурсора допамин-levodopa-в пациента учтено очень логически терапией в виду того что levodopa отражает через барьер кров-мозга, куда оно поворачивает в допамин и нормализует уровень допамина. Таким образом, levodopa останавливает или замедляет развитие паркинсонизма. Levodopa принадлежит группе в составе самые эффективные лекарства для обрабатывать тип паркинсонизма не причиненный целебными агентами. |
| Профиль безопасности |
Отрава заглатыванием. В меру токсический внутривенными и внутрибрюшинными маршрутами. Человеческие внутрирастительные влияния заглатыванием: сомнолентность, галлюцинации и передернутые восприятия, токсический психоз, изменения деятельности при мотора, атаксия, диспноэ. Экспириментально тератогенные и воспроизводственные влияния. Спорный человеческий карциноген производящ опухоли кожи. Человеческие данные по перегласовки сообщили. Антихолинергический агент используемый как анти- лекарство Parhnsonian. Нагреванный к декомпозиции оно испускает токсические перегары NOx |
| Химический синтез |
Levodopa, (-) - 3 (3,4-dihydroxyphenyl) - L-аланин (10.1.1), levorotatory изомер dioxyphenylalanine используемый как прекурсор допамина. Немного путей получать levodopa используя полусинтетический подход, который состоит из микробиологического гидроксилирования L-тирозина (10.1.1), так же, как снабжать чисто синтетический подход.
Оксидация L-тирозина, для выборочного введения группы гидроксила на C3 tyro? кольцо синуса, можно выполнить в чисто синтетическом образе путем использование смеси гидрактора? перекись и утюг gen (II) сульфатизируют смесь в воде как оксидант с постоянным присутсвием кислорода.

Третий метод синтеза levodopa состоит из ацетилирования тирозина используя acetylchlo? езда в присутствии к хлористому алюминию и последующее оксидативное deacylation сформированного acetyltyrosine 3 (10.1.2) используя перекись водорода в решении окисоводопода натрия.
 |
| Методы очищения |
Правоподобные примеси ванилин, гиппуровая кислота, aminotyrosine 3 tyrosine и 3. ДОПА рекристаллизует от больших томов H2O формируя бесцветные белые иглы; своя растворимость в H2O 0,165%, но она неразрешима в EtOH, *C6H6, CHCl3, и EtOAc. Также выкристаллизовывайте его путем растворять его внутри разбавьте HCl и добавляющ разбавьте амиак для того чтобы дать пэ-аш 5, под N2. Альтернативно, выкристаллизовывайте его от разбавьте водное EtOH. Оно быстро окислен в воздухе когда влажный, и затмевает, особенно в щелочном растворе. Высушите его в - vacuo на 70o в темноте, и сохраните оно в темном контейнере предпочтительно под N2. Он имеет на 220.5nm (журнале 3,79) и 280nm (журнале 3,42) в максимальном HCl 0.001N. [Yamada и др. Chem Pharm Bull Jpn 10 693 1962, протоколы 56 Bretschneider и др. Helv Chim 2857 1973, НАЦИОНАЛЬНЫЙ ВОЕННЫЙ ПРЕДСТАВИТЕЛЬ: Jardetzky & Biol Chem 233 Jardetzky j 383 1958, Beilstein 4 IV 2492, 2493.] |
| |
| Продукты и сырье подготовки Levodopa |
|